Interaktioner mellan virus och värd som begränsar infektioner
Kort beskrivning
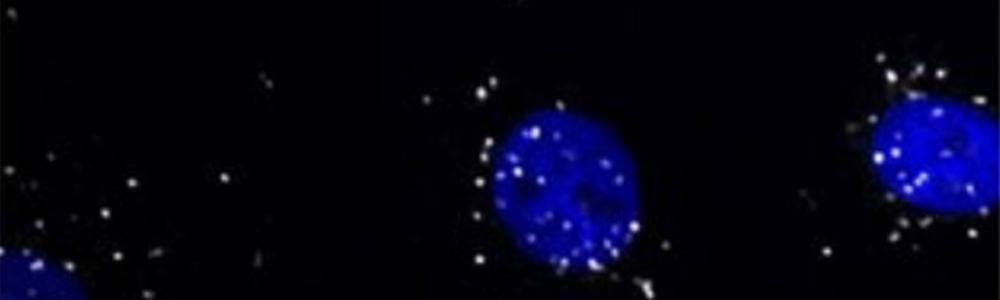
Michaels Kanns forskningsgrupp försöker förstå de interaktioner som begränsar virusinfektioner. Vi analyserar tre olika virus, adeno-associerade virus (AAV), hepatit B-virus (HBV) och SARS-CoV-2. Medan AAV och HBV undersöks med hjälp av realtidsmikroskopi, analyseras HBV och SARS-CoV-2 med hjälp av signaturer i deras genomer, som visar på begränsningar av värdens medfödda immunförsvar.
Vi analyserar tre virus som är biologiskt och medicinskt olika: AAVs (adeno-associerade virus) är enkelsträngade DNA-virus som inte orsakar någon sjukdom, trots att de orsakar kroniska infektioner. De är därför den viktigaste plattformen för genterapi: Det finns för närvarande tre godkända läkemedel för behandling av sällsynta genetiska sjukdomar. De är dock mycket ineffektiva, vilket innebär att det krävs hundratals virus för att infektera en enda cell. Det är troligt att ineffektiviteten beror på ineffektiv transport av genomet från cellperiferin till cellkärnan och inte på att värdarnas medfödda immunförsvar motverkar infektionen. Målet med vår forskning är att förstå de begränsande faktorerna med hjälp av realtidsmikroskopi i kombination med genomomfattande screening av begränsande värdfaktorer.
HBV (hepatitis B virus) - till skillnad från AAV - är patogena och orsakar akuta, fulminanta och kroniska infektioner, som spontant elimineras med en låg frekvens på ca 1 % per år. Kroniska infektioner leder till levercirros och är den främsta orsaken till hepatocellulärt karcinom hos människor. HBV har också ett DNA-genom, men det är delvis dubbelsträngat och däremot extremt effektivt. Liksom AAV replikeras det i cellens kärna och kärn-DNA är mycket stabilt och kan inte angripas av nuvarande behandlingar. Vårt mål är att förstå virusets effektivitet och genomets öde vid celldelning. Vi tar upp dessa frågor med hjälp av realtidsmikroskopi på samma sätt som i våra studier av AAV. Vi undersöker vidare delar av det medfödda immunsvaret, vilket kan leda till spontan eliminering av kronisk infektion. Vi fokuserar på deamineringar av virusgenomet, som kan introducera ett kritiskt antal mutationer, vilket leder till muterat HBV med lägre fitness. Detta analyseras genom djupsekvensering av hela genomet av hepadnavirala genomer och genom att korrelera resultaten med kliniska parametrar hos patienterna.
På liknande sätt analyserar vi deaminering av SARS-CoV-2, som är ett RNA-virus som uteslutande replikerar i cytoplasman. Vi visade nyligen att ökad deaminering är korrelerad med en minskad virusbelastning och med inflammation i värden.
Michael Kann
Gruppledare
Tillhörighet:
Avdelningen för infektionssjukdomar,
Institutionen för biomedicin
Gruppmedlemmar
Maria Johansson
Gustaf Rydell
Luisa Fernanda
Bustamante Jaramillo
Joshua Fingal